急性大動脈スーパーネットワーク
最新の診断と治療
急性大動脈解離は、突然死の原因として心筋梗塞に次いで多く、上行大動脈に解離をきたすスタンフォードA型の半数以上は心嚢へ破裂し、心タンポナーデにより病院搬送前に死亡します。したがって早期診断と緊急手術が救命のカギになります。
確定診断はCT検査により行います。CT画像から、解離の存在だけでなく、解離の形態、進展、エントリー・リエントリーの同定、さらには破裂や臓器虚血の有無を評価します (図1)。単純CT、造影CT(早期相および後期相)の撮像が基本です。
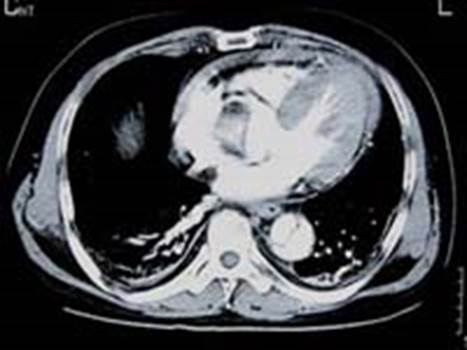
図1 偽腔開存A型。心嚢液貯留ならびに下行大動脈の二腔構造が認められる
大動脈を構成する3層は内膜、中膜、外膜ですが、石灰化は一般に内膜に生じることから、単純CTで内膜石灰化の偏位が認められれば、石灰化内膜と外膜の間が偽腔として診断できます(図2)。
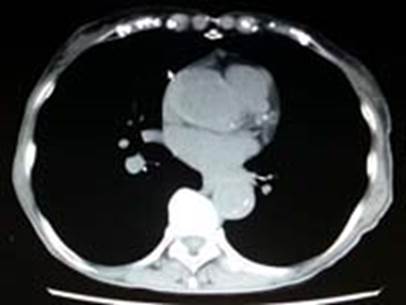
図2 単純CTによる診断。下行大動脈の石灰化内膜と外膜の間が偽腔である。
偽腔閉塞型の急性期には偽腔が高濃度域として認められます(図3)。造影CT早期相では、偽腔開存型では典型的な二腔構造を(図4)、偽腔閉塞型では造影されない偽腔が認められます(図5)。偽腔開存型解離の中に偽腔血流が非常に遅い場合があり、造影早期相では偽腔が造影されず、後期相で造影剤の流入を認める症例があるため(図6)、可能な限り造影後期相までの撮像が望まれます。
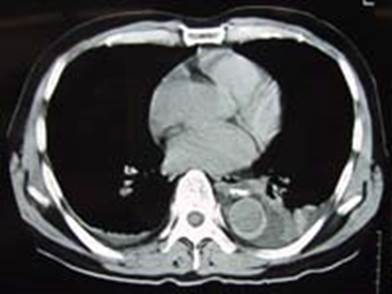
図3 偽腔閉塞B型急性期の単純CT。血栓化偽腔は発症直後を除き亜急性期まで
単純CTにおいてhigh densityを示す。
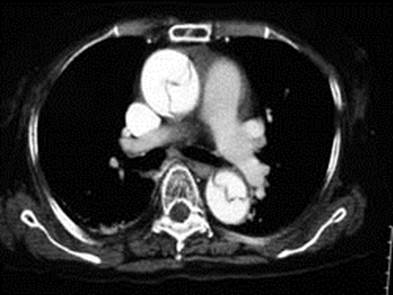
図4 偽腔開存型の造影CT。上行大動脈ならびに下行大動脈に二腔構造が認められる。
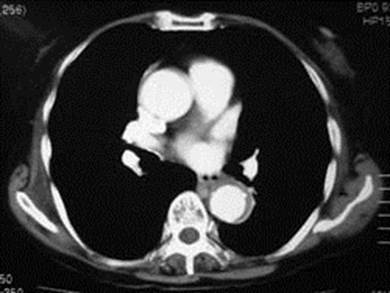
図5.偽腔閉塞B型の造影CT。下行大動脈に造影されない偽腔が認められる。
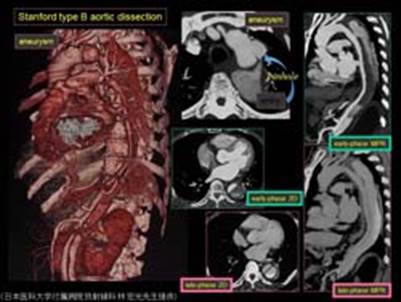
図6.偽腔開存B型の造影CT。造影早期相では偽腔の造影効果に乏しいが、
後期相では偽腔全体に造影効果が認められる。
初期治療は降圧、脈拍数コントロール、鎮痛および安静です。降圧目標は収縮期血圧100~120mmHgとし、カルシウム拮抗薬の持続静注とβ遮断薬静注を併用します。脈拍数は60~70/分前後に低下させます。外来から少なくとも入院までは絶対安静で、痛みは降圧の妨げとなるので、塩酸モルヒネもしくはブプレノルフィンを呼吸抑制に注意しながら緩除に静注します。
急性期治療方針は解離の型によって異なり、一般的に「偽腔閉塞A型」、「偽腔開存B型」のように偽腔の状態とスタンフォード分類との組み合わせで4群に分類し決定します(表)。偽腔開存A型は緊急手術が原則(図7)、偽腔閉塞A型では最大上行径が50mm以上、あるいは偽腔径が11mm以上で準緊急もしくは緊急で手術、それ以外は症例に応じて手術適応とタイミングを検討します。B型は偽腔の開存閉塞を問わず保存的に治療しますが、致死的合併症(大動脈破裂、腸管虚血、下肢虚血など)があれば緊急で侵襲的治療を行います。
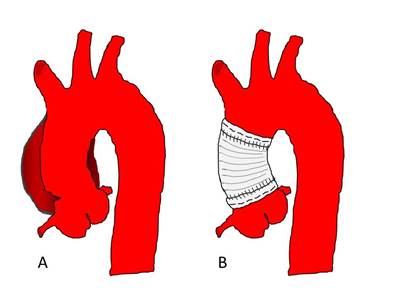
図7 人工血管置換術。上行大動脈の解離部分を人工血管に置き換える
表.解離の型別による治療方針
スタンフォードA型 スタンフォードB型
偽腔開存型 緊急手術 保存的治療(破裂や臓器虚血合併では手術)
偽腔閉塞型 心タンポナーデ、 保存的治療(破裂や臓器虚血合併では手術)
最大上行径≧50mmまたは
偽腔径≧11mmで手術
東京都CCUネットワークでは急性大動脈解離の緊急診療の効率化を目指し、急性大動脈スーパーネットワークを運用しています。とくに病院間転送の活発化を含む、24時間緊急手術が可能な重点病院への積極的患者集積を企図しています。自施設で手術が不可能である場合、あるいは厳格な全身管理ができない場合には、急性大動脈スーパーネットワークを利用して可及的速やかに転送ください。
